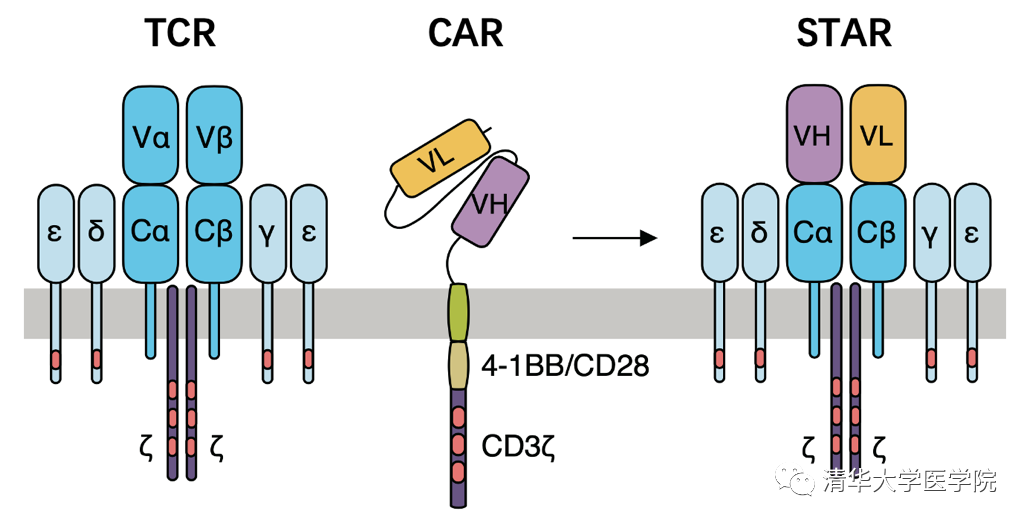
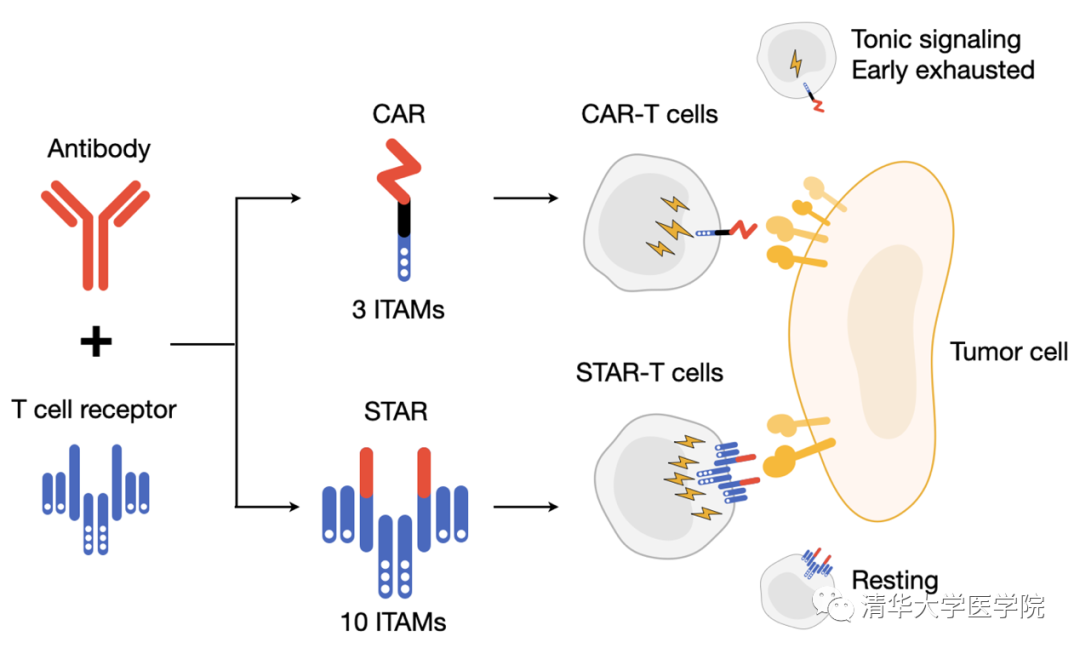
清華大學(xué)醫(yī)學(xué)院林欣團(tuán)隊(duì)在《科學(xué)轉(zhuǎn)化醫(yī)學(xué)》發(fā)文報(bào)道新型CAR-T細(xì)胞抗實(shí)體腫瘤的作用和機(jī)制
原文鏈接:
https://stm.sciencemag.org/content/13/586/eabb5191
來(lái)源:清華大學(xué)醫(yī)學(xué)院




原文鏈接:
https://stm.sciencemag.org/content/13/586/eabb5191
來(lái)源:清華大學(xué)醫(yī)學(xué)院

